中国黄金矿产资源开发及矿产品供需形势分析
1
2009
... 我国现已探明的黄金地质储量中,约有1 200 t属于难处理金矿资源,约占探明储量的1/4[1],其中硫化矿包裹微细粒浸染型金矿是主要的难处理金矿类型.由于此类金矿中金以微细粒状态包裹于硫化矿物中,所以浸出提金前必须先预处理以打开硫化物包裹.目前,国内外对含硫砷难浸金矿的预氧化处理方法大致可划分为三大类:焙烧氧化法、生物氧化法和湿法化学氧化法.焙烧氧化法的工业应用最广泛,但其在生产过程中存在重大缺陷:一是焙烧过程不但成本高,而且产生大量硫砷氧化物,这些氧化物排入空气中,会产生严重污染;二是后续的氰化浸出过程中使用剧毒氰化物,排出的废水及尾渣中氰化物的残留同样存在毒害污染问题.生物氧化法具有生产环境友好、适应性强和生产工艺运行稳定可靠等优点,但也存在氧化周期长、工艺设备要求高以及后续氰化浸出需调节碱度等缺点,直接导致生产成本较高.化学氧化法可依据矿浆pH值的不同大致划分为碱法和酸法2种预处理方法,依据反应压力条件的不同又可划分为常压预处理和热压预处理.酸法及热压法由于需要加压、加温和酸性等苛刻条件,存在成本高、设备要求高(耐酸腐蚀)、过程难控制(存在高压危险)、废液循环利用技术不成熟及环境污染等缺点,因此,生产中较少得到大规模应用.但碱法常温常压预氧化工艺由于对设备要求低、生产成本低、过程易控制及环境污染小等优点,近年来成为研究热点,具有较好的开发应用前景. ...
中国黄金矿产资源开发及矿产品供需形势分析
1
2009
... 我国现已探明的黄金地质储量中,约有1 200 t属于难处理金矿资源,约占探明储量的1/4[1],其中硫化矿包裹微细粒浸染型金矿是主要的难处理金矿类型.由于此类金矿中金以微细粒状态包裹于硫化矿物中,所以浸出提金前必须先预处理以打开硫化物包裹.目前,国内外对含硫砷难浸金矿的预氧化处理方法大致可划分为三大类:焙烧氧化法、生物氧化法和湿法化学氧化法.焙烧氧化法的工业应用最广泛,但其在生产过程中存在重大缺陷:一是焙烧过程不但成本高,而且产生大量硫砷氧化物,这些氧化物排入空气中,会产生严重污染;二是后续的氰化浸出过程中使用剧毒氰化物,排出的废水及尾渣中氰化物的残留同样存在毒害污染问题.生物氧化法具有生产环境友好、适应性强和生产工艺运行稳定可靠等优点,但也存在氧化周期长、工艺设备要求高以及后续氰化浸出需调节碱度等缺点,直接导致生产成本较高.化学氧化法可依据矿浆pH值的不同大致划分为碱法和酸法2种预处理方法,依据反应压力条件的不同又可划分为常压预处理和热压预处理.酸法及热压法由于需要加压、加温和酸性等苛刻条件,存在成本高、设备要求高(耐酸腐蚀)、过程难控制(存在高压危险)、废液循环利用技术不成熟及环境污染等缺点,因此,生产中较少得到大规模应用.但碱法常温常压预氧化工艺由于对设备要求低、生产成本低、过程易控制及环境污染小等优点,近年来成为研究热点,具有较好的开发应用前景. ...
难浸含砷金精矿的碱性常温常压强化预氧化工艺工业化研究
1
2004
... 在以往的金精矿碱法预氧化研究中发现,当氧化环境适宜时,在硫化矿物被氧化的同时,金也有大量溶出现象,经对含金贵液进行成分分析,发现贵液中有Sx2-、S2O32-、AsS33-、SO42-和AsO43-等离子存在.经过查阅国内外资料,发现部分文献也有对这一现象的描述.孟宇群等[2]在对难浸含砷金精矿的碱性常温常压强化预氧化研究中发现,经过54 h预氧化后,金浸出率达到74.8%.Wu等[3]研究发现,在碱性溶液中,硫化物很容易被氧化成具有溶金作用的多硫化物和硫代硫酸盐.Jeffrey等[4]研究指出,硫可以在碱性条件下与金(I)阳离子形成稳定的配合物.因此,对于金精矿预氧化过程中金的溶出现象,很容易推测出是硫化矿物氧化生成了硫代硫酸盐等多硫化物并产生浸金作用的结果.这说明只要条件适合,不需要另外加入溶解金的配位基团,利用硫化矿自身氧化产生的浸金成分就能溶解提取金. ...
难浸含砷金精矿的碱性常温常压强化预氧化工艺工业化研究
1
2004
... 在以往的金精矿碱法预氧化研究中发现,当氧化环境适宜时,在硫化矿物被氧化的同时,金也有大量溶出现象,经对含金贵液进行成分分析,发现贵液中有Sx2-、S2O32-、AsS33-、SO42-和AsO43-等离子存在.经过查阅国内外资料,发现部分文献也有对这一现象的描述.孟宇群等[2]在对难浸含砷金精矿的碱性常温常压强化预氧化研究中发现,经过54 h预氧化后,金浸出率达到74.8%.Wu等[3]研究发现,在碱性溶液中,硫化物很容易被氧化成具有溶金作用的多硫化物和硫代硫酸盐.Jeffrey等[4]研究指出,硫可以在碱性条件下与金(I)阳离子形成稳定的配合物.因此,对于金精矿预氧化过程中金的溶出现象,很容易推测出是硫化矿物氧化生成了硫代硫酸盐等多硫化物并产生浸金作用的结果.这说明只要条件适合,不需要另外加入溶解金的配位基团,利用硫化矿自身氧化产生的浸金成分就能溶解提取金. ...
Basic theory and optimization of gold containing antimony concentrate leaching by alkaline sulfide
1
2019
... 在以往的金精矿碱法预氧化研究中发现,当氧化环境适宜时,在硫化矿物被氧化的同时,金也有大量溶出现象,经对含金贵液进行成分分析,发现贵液中有Sx2-、S2O32-、AsS33-、SO42-和AsO43-等离子存在.经过查阅国内外资料,发现部分文献也有对这一现象的描述.孟宇群等[2]在对难浸含砷金精矿的碱性常温常压强化预氧化研究中发现,经过54 h预氧化后,金浸出率达到74.8%.Wu等[3]研究发现,在碱性溶液中,硫化物很容易被氧化成具有溶金作用的多硫化物和硫代硫酸盐.Jeffrey等[4]研究指出,硫可以在碱性条件下与金(I)阳离子形成稳定的配合物.因此,对于金精矿预氧化过程中金的溶出现象,很容易推测出是硫化矿物氧化生成了硫代硫酸盐等多硫化物并产生浸金作用的结果.这说明只要条件适合,不需要另外加入溶解金的配位基团,利用硫化矿自身氧化产生的浸金成分就能溶解提取金. ...
A fundamental study of the alkaline sulfide leaching of gold
2
2003
... 在以往的金精矿碱法预氧化研究中发现,当氧化环境适宜时,在硫化矿物被氧化的同时,金也有大量溶出现象,经对含金贵液进行成分分析,发现贵液中有Sx2-、S2O32-、AsS33-、SO42-和AsO43-等离子存在.经过查阅国内外资料,发现部分文献也有对这一现象的描述.孟宇群等[2]在对难浸含砷金精矿的碱性常温常压强化预氧化研究中发现,经过54 h预氧化后,金浸出率达到74.8%.Wu等[3]研究发现,在碱性溶液中,硫化物很容易被氧化成具有溶金作用的多硫化物和硫代硫酸盐.Jeffrey等[4]研究指出,硫可以在碱性条件下与金(I)阳离子形成稳定的配合物.因此,对于金精矿预氧化过程中金的溶出现象,很容易推测出是硫化矿物氧化生成了硫代硫酸盐等多硫化物并产生浸金作用的结果.这说明只要条件适合,不需要另外加入溶解金的配位基团,利用硫化矿自身氧化产生的浸金成分就能溶解提取金. ...
... 朱国才等[44]在热力学分析的基础上,提出了用元素硫歧化产物浸金的工艺路线,研究认为对于元素硫歧化形成的硫代硫酸盐及多硫化物混合体系而言,在无外加氧化剂的条件下,其中的硫代硫酸盐对金不起浸取作用,也就是说,混合体系中有效的浸金成分为多硫化物;笔者选用山东和广东的金矿进行了试验,金浸出率达到92%.Jeffrey等[4]也得出类似研究结论,测得多硫化物浸出体系的混合电位为-515 mV,与S22-转化S2-的还原电位(-507 mV)非常接近,因此推测有效的浸出剂是多硫化物而不是硫代硫酸盐,在浸金过程中多硫化物起氧化剂的作用. ...
Removal of arsenic and sulfur from mixed ores or concentrates
1
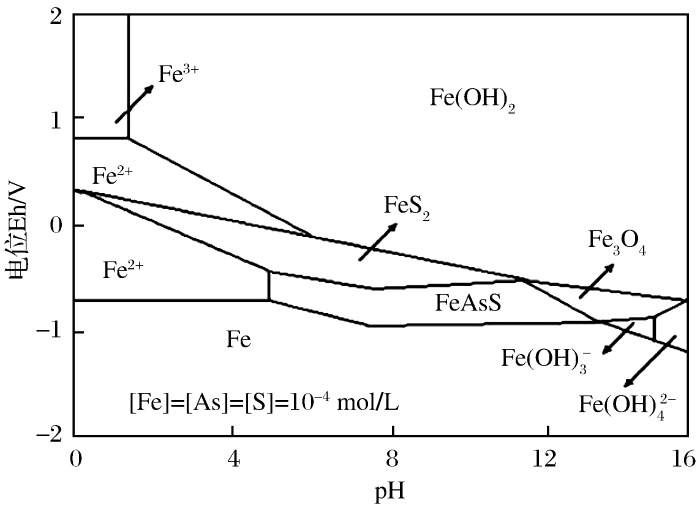
... 早在20世纪50年代,就有学者研究硫化砷矿的碱性氧化工艺并在工业上进行应用[5-7].常用的碱性氧化剂有NaOH、NaClO和CaO2等.1984年Osseo-Asare等[8]在热力学计算的基础上给出了常温下Fe-As-S体系的Eh-pH图(图1),其研究认为,在整个pH值范围内,砷黄铁矿(FeAsS)氧化的电极电位很低,一般氧化剂(如空气)就能使其氧化溶解;随着pH值的增加,氧化反应所需的电位变得更负;与黄铁矿(FeS2)相比,砷黄铁矿氧化的电位更低,比黄铁矿更易氧化. ...
Oxidation of arsenopyrite by oxygen under pressure and elevated temperature in alkali medium
1
1959
... 早在20世纪50年代,就有学者研究硫化砷矿的碱性氧化工艺并在工业上进行应用[5-7].常用的碱性氧化剂有NaOH、NaClO和CaO2等.1984年Osseo-Asare等[8]在热力学计算的基础上给出了常温下Fe-As-S体系的Eh-pH图(图1),其研究认为,在整个pH值范围内,砷黄铁矿(FeAsS)氧化的电极电位很低,一般氧化剂(如空气)就能使其氧化溶解;随着pH值的增加,氧化反应所需的电位变得更负;与黄铁矿(FeS2)相比,砷黄铁矿氧化的电位更低,比黄铁矿更易氧化. ...
Solution chemistry of cyanide leaching systems
1
1984
... 早在20世纪50年代,就有学者研究硫化砷矿的碱性氧化工艺并在工业上进行应用[5-7].常用的碱性氧化剂有NaOH、NaClO和CaO2等.1984年Osseo-Asare等[8]在热力学计算的基础上给出了常温下Fe-As-S体系的Eh-pH图(图1),其研究认为,在整个pH值范围内,砷黄铁矿(FeAsS)氧化的电极电位很低,一般氧化剂(如空气)就能使其氧化溶解;随着pH值的增加,氧化反应所需的电位变得更负;与黄铁矿(FeS2)相比,砷黄铁矿氧化的电位更低,比黄铁矿更易氧化. ...
Oxidation of Pyrite in Alkaline Solutions and Heterogeneous Equilibria of Sulfur- and Arsenic-containing Minerals in Cyanide Solutions
1
1987
... 其他研究[9-12]也表明,砷黄铁矿和黄铁矿在碱性介质中具有较低电势,不稳定,易发生氧化,结果基本一致.龙炳清等[13]和毛暗章[14]通过分析矿浆液相成分,发现有S2O32-和AsS33-存在,推测FeAsS氧化的反应机理如下: ...
Kinetics of pyrite oxidation in sodium carbonate solutions
0
1995
Study of the mechanism of electrochemical oxidation of arsenopyrite and pyrite in caustic soda solutions
0
1979
The incipient oxidation of pyrite
1
1994
... 其他研究[9-12]也表明,砷黄铁矿和黄铁矿在碱性介质中具有较低电势,不稳定,易发生氧化,结果基本一致.龙炳清等[13]和毛暗章[14]通过分析矿浆液相成分,发现有S2O32-和AsS33-存在,推测FeAsS氧化的反应机理如下: ...
FeAsS-H2O系和FeS2-H2O系的热力学分析
1
1990
... 其他研究[9-12]也表明,砷黄铁矿和黄铁矿在碱性介质中具有较低电势,不稳定,易发生氧化,结果基本一致.龙炳清等[13]和毛暗章[14]通过分析矿浆液相成分,发现有S2O32-和AsS33-存在,推测FeAsS氧化的反应机理如下: ...
FeAsS-H2O系和FeS2-H2O系的热力学分析
1
1990
... 其他研究[9-12]也表明,砷黄铁矿和黄铁矿在碱性介质中具有较低电势,不稳定,易发生氧化,结果基本一致.龙炳清等[13]和毛暗章[14]通过分析矿浆液相成分,发现有S2O32-和AsS33-存在,推测FeAsS氧化的反应机理如下: ...
高砷硫难处理金精矿浸金新工艺与理论研究
2
1997
... 其他研究[9-12]也表明,砷黄铁矿和黄铁矿在碱性介质中具有较低电势,不稳定,易发生氧化,结果基本一致.龙炳清等[13]和毛暗章[14]通过分析矿浆液相成分,发现有S2O32-和AsS33-存在,推测FeAsS氧化的反应机理如下: ...
... 毛暗章[14,17]、黎铉海等[18]用Eh-pH图和Gibbs 自由能研究分析了以NaClO为浸金剂一步法浸金的原理和浸出条件,认为在足够的碱性条件下,NaClO能将FeAsS和FeS2氧化分解,并一步将金浸出.在Cl-Au-H2O 体系中,由于Au3+和Cl- 形成稳定的配合物,Au氧化的标准电极电位由原来的1.50 V下降至1.00 V,如果溶液中[Cl-]=2 mol/L,[Au3+]=10-2 mol/L,电极电位下降至0.92 V,当pH>5时,AuCl4-能在溶液中稳定存在.当体系中pH值提高时,AuCl4-稳定性变差,逐渐以Au(OH)3形式沉淀.当继续碱化时,Au(OH)3表现出两性复而溶解,形成了H2AuO3-和HAuO32-;当pH>13时,H2AuO3-和HAuO32-是金的主要存在形式.NaClO碱性条件下金的溶解机理如下: ...
高砷硫难处理金精矿浸金新工艺与理论研究
2
1997
... 其他研究[9-12]也表明,砷黄铁矿和黄铁矿在碱性介质中具有较低电势,不稳定,易发生氧化,结果基本一致.龙炳清等[13]和毛暗章[14]通过分析矿浆液相成分,发现有S2O32-和AsS33-存在,推测FeAsS氧化的反应机理如下: ...
... 毛暗章[14,17]、黎铉海等[18]用Eh-pH图和Gibbs 自由能研究分析了以NaClO为浸金剂一步法浸金的原理和浸出条件,认为在足够的碱性条件下,NaClO能将FeAsS和FeS2氧化分解,并一步将金浸出.在Cl-Au-H2O 体系中,由于Au3+和Cl- 形成稳定的配合物,Au氧化的标准电极电位由原来的1.50 V下降至1.00 V,如果溶液中[Cl-]=2 mol/L,[Au3+]=10-2 mol/L,电极电位下降至0.92 V,当pH>5时,AuCl4-能在溶液中稳定存在.当体系中pH值提高时,AuCl4-稳定性变差,逐渐以Au(OH)3形式沉淀.当继续碱化时,Au(OH)3表现出两性复而溶解,形成了H2AuO3-和HAuO32-;当pH>13时,H2AuO3-和HAuO32-是金的主要存在形式.NaClO碱性条件下金的溶解机理如下: ...
Alkaline leaching of refractory gold arseno-sulphide concentrates
1
1993
... Rossovsky[15]和王淀佐等[16]通过热力学分析认为,在碱性介质中,在以NaClO为氧化剂的作用下,矿物中的S和As首先氧化成S2O32-和AsS33-,然后氧化成SO42-和AsO43-,反应后的渣中基本不存在单质硫. ...
FeAsS、FeS2、Au的NaClO-NaOH体系热力学分析与金的一步浸出
1
1998
... Rossovsky[15]和王淀佐等[16]通过热力学分析认为,在碱性介质中,在以NaClO为氧化剂的作用下,矿物中的S和As首先氧化成S2O32-和AsS33-,然后氧化成SO42-和AsO43-,反应后的渣中基本不存在单质硫. ...
FeAsS、FeS2、Au的NaClO-NaOH体系热力学分析与金的一步浸出
1
1998
... Rossovsky[15]和王淀佐等[16]通过热力学分析认为,在碱性介质中,在以NaClO为氧化剂的作用下,矿物中的S和As首先氧化成S2O32-和AsS33-,然后氧化成SO42-和AsO43-,反应后的渣中基本不存在单质硫. ...
One-step leaching of some refractory gold concentrate containing arsenic and theory analysis
1
1997
... 毛暗章[14,17]、黎铉海等[18]用Eh-pH图和Gibbs 自由能研究分析了以NaClO为浸金剂一步法浸金的原理和浸出条件,认为在足够的碱性条件下,NaClO能将FeAsS和FeS2氧化分解,并一步将金浸出.在Cl-Au-H2O 体系中,由于Au3+和Cl- 形成稳定的配合物,Au氧化的标准电极电位由原来的1.50 V下降至1.00 V,如果溶液中[Cl-]=2 mol/L,[Au3+]=10-2 mol/L,电极电位下降至0.92 V,当pH>5时,AuCl4-能在溶液中稳定存在.当体系中pH值提高时,AuCl4-稳定性变差,逐渐以Au(OH)3形式沉淀.当继续碱化时,Au(OH)3表现出两性复而溶解,形成了H2AuO3-和HAuO32-;当pH>13时,H2AuO3-和HAuO32-是金的主要存在形式.NaClO碱性条件下金的溶解机理如下: ...
含砷难浸金矿次氯酸钠一步法浸金理论与技术
1
2000
... 毛暗章[14,17]、黎铉海等[18]用Eh-pH图和Gibbs 自由能研究分析了以NaClO为浸金剂一步法浸金的原理和浸出条件,认为在足够的碱性条件下,NaClO能将FeAsS和FeS2氧化分解,并一步将金浸出.在Cl-Au-H2O 体系中,由于Au3+和Cl- 形成稳定的配合物,Au氧化的标准电极电位由原来的1.50 V下降至1.00 V,如果溶液中[Cl-]=2 mol/L,[Au3+]=10-2 mol/L,电极电位下降至0.92 V,当pH>5时,AuCl4-能在溶液中稳定存在.当体系中pH值提高时,AuCl4-稳定性变差,逐渐以Au(OH)3形式沉淀.当继续碱化时,Au(OH)3表现出两性复而溶解,形成了H2AuO3-和HAuO32-;当pH>13时,H2AuO3-和HAuO32-是金的主要存在形式.NaClO碱性条件下金的溶解机理如下: ...
含砷难浸金矿次氯酸钠一步法浸金理论与技术
1
2000
... 毛暗章[14,17]、黎铉海等[18]用Eh-pH图和Gibbs 自由能研究分析了以NaClO为浸金剂一步法浸金的原理和浸出条件,认为在足够的碱性条件下,NaClO能将FeAsS和FeS2氧化分解,并一步将金浸出.在Cl-Au-H2O 体系中,由于Au3+和Cl- 形成稳定的配合物,Au氧化的标准电极电位由原来的1.50 V下降至1.00 V,如果溶液中[Cl-]=2 mol/L,[Au3+]=10-2 mol/L,电极电位下降至0.92 V,当pH>5时,AuCl4-能在溶液中稳定存在.当体系中pH值提高时,AuCl4-稳定性变差,逐渐以Au(OH)3形式沉淀.当继续碱化时,Au(OH)3表现出两性复而溶解,形成了H2AuO3-和HAuO32-;当pH>13时,H2AuO3-和HAuO32-是金的主要存在形式.NaClO碱性条件下金的溶解机理如下: ...
Advances in mineral processing
1
1986
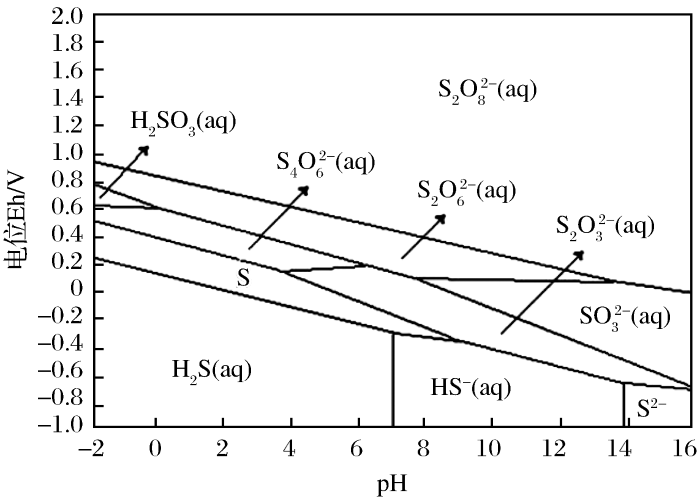
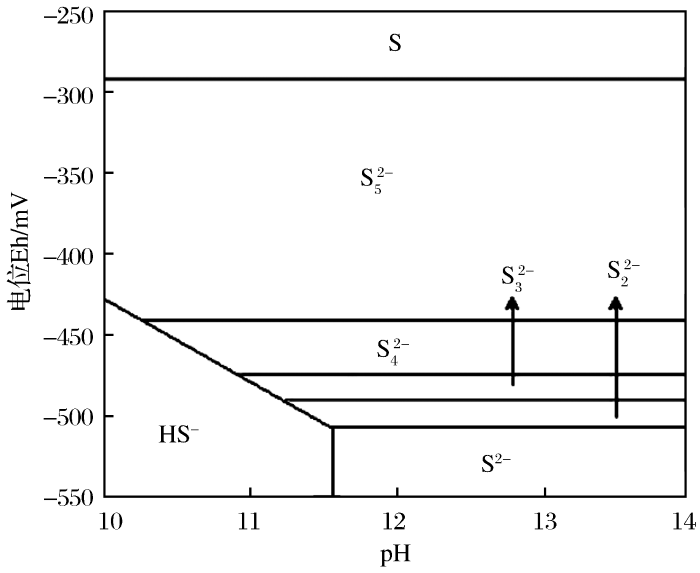
... Ernest[19]给出了常温下S-H2O体系Eh-pH图(图2).当pH<7时,元素S0能稳定存在,即酸性条件浸出时,会有S0产生;当pH>7时,元素S0不稳定,会发生转化,FeS2或FeAsS中的S在氧化为SO42-的过程中,硫的价态转变为:S2-→S-→S0→S2+→S4+→S6+.Pourbaix等[20]利用StabCal热化学数据包软件绘制了碱性溶液中硫的亚稳态Eh-pH图(图3).硫化物/多硫化物的Eh-pH图表明,硫化物(S2-)不是氧化剂,因为硫化物的氧化态是所有硫中最低的.多硫化物是一种潜在的氧化剂,因为它可以从高分子量的多硫化物还原为低分子量的多硫化物或硫化物. ...
Potential-pH equilibrium diagrams for the system S-H2O from 25 to 150 ℃:Influence of access of oxygen in sulphide solutions
1
1992
... Ernest[19]给出了常温下S-H2O体系Eh-pH图(图2).当pH<7时,元素S0能稳定存在,即酸性条件浸出时,会有S0产生;当pH>7时,元素S0不稳定,会发生转化,FeS2或FeAsS中的S在氧化为SO42-的过程中,硫的价态转变为:S2-→S-→S0→S2+→S4+→S6+.Pourbaix等[20]利用StabCal热化学数据包软件绘制了碱性溶液中硫的亚稳态Eh-pH图(图3).硫化物/多硫化物的Eh-pH图表明,硫化物(S2-)不是氧化剂,因为硫化物的氧化态是所有硫中最低的.多硫化物是一种潜在的氧化剂,因为它可以从高分子量的多硫化物还原为低分子量的多硫化物或硫化物. ...
Disproportionation of aqueous sulfur and sulfide:Kinetics of polysulfide decomposition
1
1997
... Licht等[21]和Kleinjan等[22]研究了多硫化物离子在碱性水溶液中的氧化动力学,结果表明,多硫阴离子可以进一步自氧化生成单质硫和硫代硫酸盐.Hyland等[23]和Mycroft等[24]研究硫化物的氧化时曾提出过反应机理,认为S2-氧化可能生成元素S的氧化物如S2O32-、SO32-和SO42-等离子,其中S2O32-进一步氧化成SO32-和SO42-是一个极慢的过程,常温下氧化的半衰期为8 d.Dhawale[25]研究指出硫代硫酸盐在无氧水溶液中是稳定的.在常温常压下,如果没有Cu2+的催化作用,在碱性溶液中硫代硫酸盐的降解速度极为缓慢.S-H2O体系的Eh-pH图表明硫代硫酸盐的金属配合物在相对较宽的电位/pH范围内是稳定的[26]. ...
Kinetics of the chemical oxidation of polysulfide anions in aqueous solution
1
2005
... Licht等[21]和Kleinjan等[22]研究了多硫化物离子在碱性水溶液中的氧化动力学,结果表明,多硫阴离子可以进一步自氧化生成单质硫和硫代硫酸盐.Hyland等[23]和Mycroft等[24]研究硫化物的氧化时曾提出过反应机理,认为S2-氧化可能生成元素S的氧化物如S2O32-、SO32-和SO42-等离子,其中S2O32-进一步氧化成SO32-和SO42-是一个极慢的过程,常温下氧化的半衰期为8 d.Dhawale[25]研究指出硫代硫酸盐在无氧水溶液中是稳定的.在常温常压下,如果没有Cu2+的催化作用,在碱性溶液中硫代硫酸盐的降解速度极为缓慢.S-H2O体系的Eh-pH图表明硫代硫酸盐的金属配合物在相对较宽的电位/pH范围内是稳定的[26]. ...
An XPS study of gold deposition at low temperature on sulfide minerals:Reducing agents
1
1989
... Licht等[21]和Kleinjan等[22]研究了多硫化物离子在碱性水溶液中的氧化动力学,结果表明,多硫阴离子可以进一步自氧化生成单质硫和硫代硫酸盐.Hyland等[23]和Mycroft等[24]研究硫化物的氧化时曾提出过反应机理,认为S2-氧化可能生成元素S的氧化物如S2O32-、SO32-和SO42-等离子,其中S2O32-进一步氧化成SO32-和SO42-是一个极慢的过程,常温下氧化的半衰期为8 d.Dhawale[25]研究指出硫代硫酸盐在无氧水溶液中是稳定的.在常温常压下,如果没有Cu2+的催化作用,在碱性溶液中硫代硫酸盐的降解速度极为缓慢.S-H2O体系的Eh-pH图表明硫代硫酸盐的金属配合物在相对较宽的电位/pH范围内是稳定的[26]. ...
Detection of sulphur and polysulphides on electrochemically oxidized pyrite surfaces by X-ray photoelectron spectroscopy and Raman spectroscopy
1
1990
... Licht等[21]和Kleinjan等[22]研究了多硫化物离子在碱性水溶液中的氧化动力学,结果表明,多硫阴离子可以进一步自氧化生成单质硫和硫代硫酸盐.Hyland等[23]和Mycroft等[24]研究硫化物的氧化时曾提出过反应机理,认为S2-氧化可能生成元素S的氧化物如S2O32-、SO32-和SO42-等离子,其中S2O32-进一步氧化成SO32-和SO42-是一个极慢的过程,常温下氧化的半衰期为8 d.Dhawale[25]研究指出硫代硫酸盐在无氧水溶液中是稳定的.在常温常压下,如果没有Cu2+的催化作用,在碱性溶液中硫代硫酸盐的降解速度极为缓慢.S-H2O体系的Eh-pH图表明硫代硫酸盐的金属配合物在相对较宽的电位/pH范围内是稳定的[26]. ...
Thiosufate:An interesting sulfur oxoanion that is useful in both medicine and industry-but is implicated in corrosion
1
1993
... Licht等[21]和Kleinjan等[22]研究了多硫化物离子在碱性水溶液中的氧化动力学,结果表明,多硫阴离子可以进一步自氧化生成单质硫和硫代硫酸盐.Hyland等[23]和Mycroft等[24]研究硫化物的氧化时曾提出过反应机理,认为S2-氧化可能生成元素S的氧化物如S2O32-、SO32-和SO42-等离子,其中S2O32-进一步氧化成SO32-和SO42-是一个极慢的过程,常温下氧化的半衰期为8 d.Dhawale[25]研究指出硫代硫酸盐在无氧水溶液中是稳定的.在常温常压下,如果没有Cu2+的催化作用,在碱性溶液中硫代硫酸盐的降解速度极为缓慢.S-H2O体系的Eh-pH图表明硫代硫酸盐的金属配合物在相对较宽的电位/pH范围内是稳定的[26]. ...
Thiosulfate leaching of gold—A review
1
2001
... Licht等[21]和Kleinjan等[22]研究了多硫化物离子在碱性水溶液中的氧化动力学,结果表明,多硫阴离子可以进一步自氧化生成单质硫和硫代硫酸盐.Hyland等[23]和Mycroft等[24]研究硫化物的氧化时曾提出过反应机理,认为S2-氧化可能生成元素S的氧化物如S2O32-、SO32-和SO42-等离子,其中S2O32-进一步氧化成SO32-和SO42-是一个极慢的过程,常温下氧化的半衰期为8 d.Dhawale[25]研究指出硫代硫酸盐在无氧水溶液中是稳定的.在常温常压下,如果没有Cu2+的催化作用,在碱性溶液中硫代硫酸盐的降解速度极为缓慢.S-H2O体系的Eh-pH图表明硫代硫酸盐的金属配合物在相对较宽的电位/pH范围内是稳定的[26]. ...
The role of ligands and oxidants in thiosulfate leaching of gold
1
2005
... 大量的研究表明[27-28],硫代硫酸盐中的硫是一种亚稳态硫,而在碱性水溶液或矿浆中又很难避免氧的存在,因此硫代硫酸盐在金浸出过程中一定会发生氧化作用,最终氧化生成多种硫产物,如亚硫酸盐、硫酸盐和多硫酸盐等. ...
A review of factors affecting gold leaching in non-ammoniacal thiosulfate solutions including degradation and in-situ generation of thiosulfate
1
2018
... 大量的研究表明[27-28],硫代硫酸盐中的硫是一种亚稳态硫,而在碱性水溶液或矿浆中又很难避免氧的存在,因此硫代硫酸盐在金浸出过程中一定会发生氧化作用,最终氧化生成多种硫产物,如亚硫酸盐、硫酸盐和多硫酸盐等. ...
Polysulfides do not cause passivation:Results from the dissolution of pyrite and implications for other sulfide minerals
1
2013
... 关于硫化矿物氧化前人已做了大量研究工作,研究发现硫化矿氧化过程中存在钝化现象.Holmes等[29]认为,在黄铁矿的碱性氧化溶解过程中,产生的多硫化物并不会形成钝化层从而阻碍黄铁矿继续溶解.Mehdi等[30]进行了难处理金矿在NaClO-NaCl溶液体系中硫化物氧化和同步浸出金的研究,发现在初始pH=11、Ca(OCl)2浓度为200 g/L和NaCl浓度为200 g/L的条件下,金的浸出率在2 h内即可达到约82%.作者通过SEM和EDX分析,发现氧化30 min后,黄铁矿颗粒表面开始有Fe(OH)3薄膜生成,从而阻碍了黄铁矿继续氧化溶解和金的浸出(图4). ...
Simultaneous sulfide oxidation and gold leaching of a refractory gold concentrate by chloride-hypochlorite solution
1
2013
... 关于硫化矿物氧化前人已做了大量研究工作,研究发现硫化矿氧化过程中存在钝化现象.Holmes等[29]认为,在黄铁矿的碱性氧化溶解过程中,产生的多硫化物并不会形成钝化层从而阻碍黄铁矿继续溶解.Mehdi等[30]进行了难处理金矿在NaClO-NaCl溶液体系中硫化物氧化和同步浸出金的研究,发现在初始pH=11、Ca(OCl)2浓度为200 g/L和NaCl浓度为200 g/L的条件下,金的浸出率在2 h内即可达到约82%.作者通过SEM和EDX分析,发现氧化30 min后,黄铁矿颗粒表面开始有Fe(OH)3薄膜生成,从而阻碍了黄铁矿继续氧化溶解和金的浸出(图4). ...
含氧溶液中毒砂氧化溶解的XAFS研究
1
2016
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
含氧溶液中毒砂氧化溶解的XAFS研究
1
2016
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
碱性环境中黄铁矿表面反应机理研究
1
2014
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
碱性环境中黄铁矿表面反应机理研究
1
2014
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
Effect of arsenopyrite on thiosulfate leaching of gold
2
2015
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
... Nadirov等[73]制备了一种特殊的“硫/石墨”电极并使用这种电极来产生含硫的浸金剂,在碱性溶液中提取金,金的回收率达到了93%.Yang等[33]采用硫和硫化钠在加压水热条件下反应生成多硫化钠溶液,并使用该多硫化钠溶液作为浸金剂进行含金矿石的浸出,取得了较好的浸出效果,该方法对试验金矿石样品的金浸出率达到85%.唐云等[74]采用碱性热压预处理—硫代硫酸盐浸出含碳质微细粒浸染型难选原生金矿,试验结果表明,在磨矿细度为-0.025 mm粒级占82%,预处理温度为160 ℃、预处理时间为2 h、助氧剂TW用量为300 g/t、氧压为1.6 MPa、pH=12的碱性热压氧化条件下以及硫代硫酸钠用量为0.12 mol/L、硫酸铵用量为0.075 mol/L、硫酸铜用量为0.02 mol/L、pH=9、浸出时间为4 h、矿浆液固比为3∶1的浸出条件下,金浸出率为88.76%. ...
The effect of solution parameters on the thiosulfate leaching of Zarshouran refractory gold ore
1
2014
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
某难处理金精矿浸金新工艺试验研究
1
1997
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
某难处理金精矿浸金新工艺试验研究
1
1997
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
Effect of Pyrite on thiosulfate leaching of gold and the role of ammonium alcohol polyvinyl phosphate
1
2017
... 张国庆等[31] 利用 X 射线吸收精细结构(X-ray Absorption Fine Structure,XAFS)分析了毒砂氧化过程中As的形态转化.结果表明,在碱性条件下,毒砂氧化反应释放出的 Fe 快速形成了 Fe 的氧化物沉淀,包裹在毒砂的表面,阻碍毒砂继续氧化.许涛等[32] 采用 SEM、XPS 检测手段和前线轨道理论计算,对碱性环境下的黄铁矿表面反应机理进行研究.结果表明,黄铁矿中的 S、Fe、Cu 原子由晶格跃迁到表面,并氧化形成硫酸盐、氢氧化物、S0或 S8.Yang等[33]和Aazmi等[34]研究了砷黄铁矿对硫代硫酸盐浸金的影响,研究表明砷黄铁矿会显著阻碍金的浸出,研究认为主要原因有2个方面:一是砷黄铁矿促进了硫代硫酸盐分解,二是在金的表面形成了Cu2S或Cu(S2O3)35-、S、FeOOH及FeAsO4等钝化层.钝化层的不良影响可以通过添加CMC或磷酸盐得到降低或消除.邱冠周等[35]采用瓷球磨磨削方法,来消除碱性介质中金属硫化矿物氧化产生的固相产物层对化学反应的阻碍作用,金的浸出率1 h内达到96.8%.Liu等[36] 研究了黄铁矿对硫代硫酸盐浸出金的影响及醇铵聚磷酸酯(AAPP)的作用,结果表明黄铁矿对硫代硫酸盐的分解有催化作用,并能显著提高硫代硫酸盐的消耗量.黄铁矿的存在也大大减缓了金的浸出动力,降低了金的整体溶出.金溶解的减少主要是由金的表面钝化引起的,通过添加醇铵聚磷酸酯可以有效稳定溶液中的硫代硫酸盐,促进金的浸出. ...
The mechanisms of pyrite oxidation and leaching:A fundamental perspective
1
2010
... 由于硫化矿在碱性体系中的氧化产生的浸金离子主要是Sx2- 和S2O32-等多硫化物,因此,在碱性氧化体系中,载金硫化矿中金的溶解过程实际就是多硫化物浸金的过程.多硫螯合离子S22-、S32-、S42-和S52-对金离子有很强的络合能力,在合适氧化剂的配合下,或者借助于多硫离子自身的歧化,多硫化合物能够有效地溶解金[37-38].关于多硫化物浸金机理的研究较多,其中石硫合剂浸金法(LSSS)是国内首创的非氰浸金法,也属于多硫化物浸金的范畴,因为其浸金体系属于复杂的硫代硫酸盐与多硫化物的混合体系[39-40].多硫化物法浸金法具有选择性高、无污染等优点. ...
Cyanide and other lixiviant leaching systems for gold with some practical applications
1
1995
... 由于硫化矿在碱性体系中的氧化产生的浸金离子主要是Sx2- 和S2O32-等多硫化物,因此,在碱性氧化体系中,载金硫化矿中金的溶解过程实际就是多硫化物浸金的过程.多硫螯合离子S22-、S32-、S42-和S52-对金离子有很强的络合能力,在合适氧化剂的配合下,或者借助于多硫离子自身的歧化,多硫化合物能够有效地溶解金[37-38].关于多硫化物浸金机理的研究较多,其中石硫合剂浸金法(LSSS)是国内首创的非氰浸金法,也属于多硫化物浸金的范畴,因为其浸金体系属于复杂的硫代硫酸盐与多硫化物的混合体系[39-40].多硫化物法浸金法具有选择性高、无污染等优点. ...
Leaching gold and silver with Lime-Sulphur-Synthetic-Solution:PartⅠ.Synthesi-zing of LSSS and dissolving gold and silver with it
1
1992
... 由于硫化矿在碱性体系中的氧化产生的浸金离子主要是Sx2- 和S2O32-等多硫化物,因此,在碱性氧化体系中,载金硫化矿中金的溶解过程实际就是多硫化物浸金的过程.多硫螯合离子S22-、S32-、S42-和S52-对金离子有很强的络合能力,在合适氧化剂的配合下,或者借助于多硫离子自身的歧化,多硫化合物能够有效地溶解金[37-38].关于多硫化物浸金机理的研究较多,其中石硫合剂浸金法(LSSS)是国内首创的非氰浸金法,也属于多硫化物浸金的范畴,因为其浸金体系属于复杂的硫代硫酸盐与多硫化物的混合体系[39-40].多硫化物法浸金法具有选择性高、无污染等优点. ...
Leaching gold and silver with Lime-Sulphur-Synthetic-Solution:PartⅡ.Treating ores with the LSSS
1
1992
... 由于硫化矿在碱性体系中的氧化产生的浸金离子主要是Sx2- 和S2O32-等多硫化物,因此,在碱性氧化体系中,载金硫化矿中金的溶解过程实际就是多硫化物浸金的过程.多硫螯合离子S22-、S32-、S42-和S52-对金离子有很强的络合能力,在合适氧化剂的配合下,或者借助于多硫离子自身的歧化,多硫化合物能够有效地溶解金[37-38].关于多硫化物浸金机理的研究较多,其中石硫合剂浸金法(LSSS)是国内首创的非氰浸金法,也属于多硫化物浸金的范畴,因为其浸金体系属于复杂的硫代硫酸盐与多硫化物的混合体系[39-40].多硫化物法浸金法具有选择性高、无污染等优点. ...
Dissolution chemistry of gold and silver in different lixiviants
1
1988
... 多硫化物阴离子(Sx2-,x=2~5)可以通过单质硫和硫化物在碱性溶液中反应得到,在碱性溶液中多硫化物与金可以形成金硫配合物[41-42].碱性溶液中多硫化物溶解金的化学反应式一般表示为 ...
Fundamentals and applications of alkaline sulfide leaching and recovery of gold
2
2005
... 多硫化物阴离子(Sx2-,x=2~5)可以通过单质硫和硫化物在碱性溶液中反应得到,在碱性溶液中多硫化物与金可以形成金硫配合物[41-42].碱性溶液中多硫化物溶解金的化学反应式一般表示为 ...
... 一些学者研究了高温下金和硫的结合情况,结果表明在高温下金与硫能结合并以稳定形式存在.Anderson等[42]研究了温度对碱性硫化物体系中AuS-络合物稳定性的影响,Eh-pH图表明,高温下硫化金的稳定区域相对较大,因此,提高回火温度有利于金在碱性硫化物溶液中的浸出.Zhang等[88]研究提出,微波热解过程中含金硫化物生成的单质硫可以用于从自身提取金.微波预处理在无氧条件下不仅产生了用于合成浸出剂的单质硫,而且释放了包裹在硫化矿物中的金.这些研究虽然温度尚不能达到地壳运动过程中的高温,但至少说明高温对金、硫赋存状态的影响很大.Sun等[89] 通过对中国东北白云金矿的黄铁矿进行S同位素原位分析研究得出,黄铁矿及裂隙中的可见金是从富含金属的岩浆中析出的,而不是变质黄铁矿二次搬运来的.这说明硫化矿很可能在岩浆热液作用的特定条件下与金形成过金硫化合物. ...
A review of gold extraction using noncyanide lixiviants:Fundamentals,advancements,and challenges toward alkaline sulfur-containing leaching agents
1
2020
... Sun等[43]总结出了主要金硫配合物的稳定常数和标准还原电位,见表1.可知金(Ⅰ)与硫化物形成的配合物的稳定性相对大于由二硫化物或硫代硫酸盐形成的金硫配合物. ...
碱性介质中元素硫岐化产物浸金研究
1
1996
... 朱国才等[44]在热力学分析的基础上,提出了用元素硫歧化产物浸金的工艺路线,研究认为对于元素硫歧化形成的硫代硫酸盐及多硫化物混合体系而言,在无外加氧化剂的条件下,其中的硫代硫酸盐对金不起浸取作用,也就是说,混合体系中有效的浸金成分为多硫化物;笔者选用山东和广东的金矿进行了试验,金浸出率达到92%.Jeffrey等[4]也得出类似研究结论,测得多硫化物浸出体系的混合电位为-515 mV,与S22-转化S2-的还原电位(-507 mV)非常接近,因此推测有效的浸出剂是多硫化物而不是硫代硫酸盐,在浸金过程中多硫化物起氧化剂的作用. ...
碱性介质中元素硫岐化产物浸金研究
1
1996
... 朱国才等[44]在热力学分析的基础上,提出了用元素硫歧化产物浸金的工艺路线,研究认为对于元素硫歧化形成的硫代硫酸盐及多硫化物混合体系而言,在无外加氧化剂的条件下,其中的硫代硫酸盐对金不起浸取作用,也就是说,混合体系中有效的浸金成分为多硫化物;笔者选用山东和广东的金矿进行了试验,金浸出率达到92%.Jeffrey等[4]也得出类似研究结论,测得多硫化物浸出体系的混合电位为-515 mV,与S22-转化S2-的还原电位(-507 mV)非常接近,因此推测有效的浸出剂是多硫化物而不是硫代硫酸盐,在浸金过程中多硫化物起氧化剂的作用. ...
氨性硫代硫酸盐与多硫化物混合溶液氧化动力学研究
1
1996
... 朱国才等[45]还进行了硫代硫酸盐及多硫化物混合溶液在通空气条件下的氧化动力学研究,认为混合体系在通空气条件下氧化时,主要是体系中的S2-被氧化,体系中S2-先被氧化为S0,再被氧化为Sx2-,生成的多硫化物可进一步氧化成S2O32-.杨天足等[46]进行了多硫化钠浸金研究,认为在多硫化物浸金体系中,对金溶解起氧化作用的不是O2,而是多硫离子S42-和S52-,它们与Au可形成稳定的五元环或六元环螯合物,多硫离子在溶金体系中具有氧化和配位的双重作用.其反应式可表达为 ...
氨性硫代硫酸盐与多硫化物混合溶液氧化动力学研究
1
1996
... 朱国才等[45]还进行了硫代硫酸盐及多硫化物混合溶液在通空气条件下的氧化动力学研究,认为混合体系在通空气条件下氧化时,主要是体系中的S2-被氧化,体系中S2-先被氧化为S0,再被氧化为Sx2-,生成的多硫化物可进一步氧化成S2O32-.杨天足等[46]进行了多硫化钠浸金研究,认为在多硫化物浸金体系中,对金溶解起氧化作用的不是O2,而是多硫离子S42-和S52-,它们与Au可形成稳定的五元环或六元环螯合物,多硫离子在溶金体系中具有氧化和配位的双重作用.其反应式可表达为 ...
多硫化钠浸金研究
1
1992
... 朱国才等[45]还进行了硫代硫酸盐及多硫化物混合溶液在通空气条件下的氧化动力学研究,认为混合体系在通空气条件下氧化时,主要是体系中的S2-被氧化,体系中S2-先被氧化为S0,再被氧化为Sx2-,生成的多硫化物可进一步氧化成S2O32-.杨天足等[46]进行了多硫化钠浸金研究,认为在多硫化物浸金体系中,对金溶解起氧化作用的不是O2,而是多硫离子S42-和S52-,它们与Au可形成稳定的五元环或六元环螯合物,多硫离子在溶金体系中具有氧化和配位的双重作用.其反应式可表达为 ...
多硫化钠浸金研究
1
1992
... 朱国才等[45]还进行了硫代硫酸盐及多硫化物混合溶液在通空气条件下的氧化动力学研究,认为混合体系在通空气条件下氧化时,主要是体系中的S2-被氧化,体系中S2-先被氧化为S0,再被氧化为Sx2-,生成的多硫化物可进一步氧化成S2O32-.杨天足等[46]进行了多硫化钠浸金研究,认为在多硫化物浸金体系中,对金溶解起氧化作用的不是O2,而是多硫离子S42-和S52-,它们与Au可形成稳定的五元环或六元环螯合物,多硫离子在溶金体系中具有氧化和配位的双重作用.其反应式可表达为 ...
Researches on preparation and properties of sodium polysulphide as gold leaching agent
1
2017
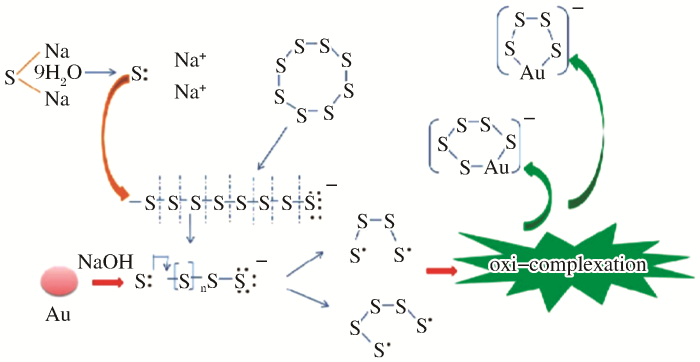
... Wen等[47]通过XRD、拉曼光谱、XPS分析和电化学分析等手段,在工艺试验及机理分析的基础上,认为四硫化物(S42-)和五硫化物(S52-)是在多硫化物溶液中浸出金的主要活性成分,并给出了多硫化物溶解金的过程示意图(图5). ...
Dissolution of gold during pyrite oxidation reaction
2
2016
... Melashvili等[48]对黄铁矿在热压氧化过程中金的溶解进行了工艺研究,认为黄铁矿在温和碱性条件下氧化的产物是硫代硫酸盐,溶金是硫代硫酸盐在起作用.在一定压力和温度(试验中为20 psi氧压和80 ℃)条件下,硫化矿氧化和金溶出同时发生.体系中溶液pH值下降则溶液电位会上升,当溶液pH>10时,金的溶解变慢;当溶液pH<8时,硫代硫酸盐开始迅速分解变为多硫酸盐或硫酸盐.在处理含金硫化矿(金和银的品位分别为95 g/t和132 g/t)的试验中,经过30 h的氧化,硫化矿氧化率达到60%以上,金和银的浸出率分别达到96%和74%.Anderson等[49-51]应用旋转电化学石英晶体微量天平(REQCM)及其他电化学手段进行了硫化矿碱性浸出(NaOH体系)的动力学及工艺方面的研究,结果表明,在载金硫化矿碱性氧化系统中,多硫化物主要起氧化作用,而硫化物是主要的浸出络合剂.金的碱性硫化浸出受温度影响较大,在一定温度范围内,随着温度的升高金的浸出率也升高.Anderson[51]还根据Arrhenius方程计算了“硫化物/多硫化物”系统的活化能(41.6 kJ /mol,大于25 kJ/ mol),认为该系统中金溶解属于化学控制过程.Sitando 等[52]利用旋转电化学石英晶体微天平对非氨态硫代硫酸盐溶液中金的溶解动力学进行了研究,结果表明金的氧化是受化学控制的,随着温度或硫代硫酸盐浓度的升高,金的氧化速度会加快. ...
... Melashvili等[48]对硫铁矿氧化过程中金的溶解情况进行了研究,结果表明,黄铁矿中硫首先被氧化成单质硫,再被氧化成硫代硫酸盐和其他硫氧阴离子,在pH<12的条件下,金的最高回收率达到96%.Xu等[72]以腐殖酸为添加剂,采用加压氧化法预处理硫化矿,利用硫氧化过程中生成的硫代硫酸盐进行浸金,金的回收率达到83.6%. ...
technology and applications
1
2014
... Melashvili等[48]对黄铁矿在热压氧化过程中金的溶解进行了工艺研究,认为黄铁矿在温和碱性条件下氧化的产物是硫代硫酸盐,溶金是硫代硫酸盐在起作用.在一定压力和温度(试验中为20 psi氧压和80 ℃)条件下,硫化矿氧化和金溶出同时发生.体系中溶液pH值下降则溶液电位会上升,当溶液pH>10时,金的溶解变慢;当溶液pH<8时,硫代硫酸盐开始迅速分解变为多硫酸盐或硫酸盐.在处理含金硫化矿(金和银的品位分别为95 g/t和132 g/t)的试验中,经过30 h的氧化,硫化矿氧化率达到60%以上,金和银的浸出率分别达到96%和74%.Anderson等[49-51]应用旋转电化学石英晶体微量天平(REQCM)及其他电化学手段进行了硫化矿碱性浸出(NaOH体系)的动力学及工艺方面的研究,结果表明,在载金硫化矿碱性氧化系统中,多硫化物主要起氧化作用,而硫化物是主要的浸出络合剂.金的碱性硫化浸出受温度影响较大,在一定温度范围内,随着温度的升高金的浸出率也升高.Anderson[51]还根据Arrhenius方程计算了“硫化物/多硫化物”系统的活化能(41.6 kJ /mol,大于25 kJ/ mol),认为该系统中金溶解属于化学控制过程.Sitando 等[52]利用旋转电化学石英晶体微天平对非氨态硫代硫酸盐溶液中金的溶解动力学进行了研究,结果表明金的氧化是受化学控制的,随着温度或硫代硫酸盐浓度的升高,金的氧化速度会加快. ...
Alkaline sulfide leaching technology;just the facts
0
2014
Alkaline sulfide gold leaching kinetics
3
2016
... Melashvili等[48]对黄铁矿在热压氧化过程中金的溶解进行了工艺研究,认为黄铁矿在温和碱性条件下氧化的产物是硫代硫酸盐,溶金是硫代硫酸盐在起作用.在一定压力和温度(试验中为20 psi氧压和80 ℃)条件下,硫化矿氧化和金溶出同时发生.体系中溶液pH值下降则溶液电位会上升,当溶液pH>10时,金的溶解变慢;当溶液pH<8时,硫代硫酸盐开始迅速分解变为多硫酸盐或硫酸盐.在处理含金硫化矿(金和银的品位分别为95 g/t和132 g/t)的试验中,经过30 h的氧化,硫化矿氧化率达到60%以上,金和银的浸出率分别达到96%和74%.Anderson等[49-51]应用旋转电化学石英晶体微量天平(REQCM)及其他电化学手段进行了硫化矿碱性浸出(NaOH体系)的动力学及工艺方面的研究,结果表明,在载金硫化矿碱性氧化系统中,多硫化物主要起氧化作用,而硫化物是主要的浸出络合剂.金的碱性硫化浸出受温度影响较大,在一定温度范围内,随着温度的升高金的浸出率也升高.Anderson[51]还根据Arrhenius方程计算了“硫化物/多硫化物”系统的活化能(41.6 kJ /mol,大于25 kJ/ mol),认为该系统中金溶解属于化学控制过程.Sitando 等[52]利用旋转电化学石英晶体微天平对非氨态硫代硫酸盐溶液中金的溶解动力学进行了研究,结果表明金的氧化是受化学控制的,随着温度或硫代硫酸盐浓度的升高,金的氧化速度会加快. ...
... [51]还根据Arrhenius方程计算了“硫化物/多硫化物”系统的活化能(41.6 kJ /mol,大于25 kJ/ mol),认为该系统中金溶解属于化学控制过程.Sitando 等[52]利用旋转电化学石英晶体微天平对非氨态硫代硫酸盐溶液中金的溶解动力学进行了研究,结果表明金的氧化是受化学控制的,随着温度或硫代硫酸盐浓度的升高,金的氧化速度会加快. ...
... 石硫合剂浸金方法(LSSS)起源于国内,属于硫化物碱性氧化浸金技术范畴.国内学者选用多种类型金矿石进行了石硫合剂浸出试验研究,发现该方法具有无毒环保、浸金速度快、适应性强、金浸出率高以及对设备材料要求低等优点.傅平丰等[53]讨论了石硫合剂法浸金的基本原理,认为LSSS 法浸金反应需在通空气及氨存在的条件下进行,浸金体系中还需加入CuSO4及Na2SO3等活化剂和稳定剂,以提高Sx2-和S2O32-的稳定性,并强化浸金过程.LSSS体系中的有效浸金成分为CaSx和 CaS2O3,溶金过程符合多硫化物及硫代硫酸盐的浸金反应.郁能文等[54]对石硫合剂(LSSS)体系进行了电化学研究,认为添加氧化剂对体系电位影响剧烈,会造成体系的稳定性降低;试验测得了稳态极化曲线,求出了LSSS体系中金电极反应活化能为16.835 kJ/mol.靳冉公等[55]对含锑难冶炼金矿碱性湿法脱锑过程中金的浸出动力学进行了研究.结果表明:温度为20~70 ℃、硫化钠浓度为20~80 g/L范围内碱性硫化钠浸出锑金矿,金的表观活化能Ea=10.948 kJ/mol.郁能文等[54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
Gold dissolution in non-ammoniacal thiosulphate solutions:Comparison of fundamentals and leaching studies
2
2015
... Melashvili等[48]对黄铁矿在热压氧化过程中金的溶解进行了工艺研究,认为黄铁矿在温和碱性条件下氧化的产物是硫代硫酸盐,溶金是硫代硫酸盐在起作用.在一定压力和温度(试验中为20 psi氧压和80 ℃)条件下,硫化矿氧化和金溶出同时发生.体系中溶液pH值下降则溶液电位会上升,当溶液pH>10时,金的溶解变慢;当溶液pH<8时,硫代硫酸盐开始迅速分解变为多硫酸盐或硫酸盐.在处理含金硫化矿(金和银的品位分别为95 g/t和132 g/t)的试验中,经过30 h的氧化,硫化矿氧化率达到60%以上,金和银的浸出率分别达到96%和74%.Anderson等[49-51]应用旋转电化学石英晶体微量天平(REQCM)及其他电化学手段进行了硫化矿碱性浸出(NaOH体系)的动力学及工艺方面的研究,结果表明,在载金硫化矿碱性氧化系统中,多硫化物主要起氧化作用,而硫化物是主要的浸出络合剂.金的碱性硫化浸出受温度影响较大,在一定温度范围内,随着温度的升高金的浸出率也升高.Anderson[51]还根据Arrhenius方程计算了“硫化物/多硫化物”系统的活化能(41.6 kJ /mol,大于25 kJ/ mol),认为该系统中金溶解属于化学控制过程.Sitando 等[52]利用旋转电化学石英晶体微天平对非氨态硫代硫酸盐溶液中金的溶解动力学进行了研究,结果表明金的氧化是受化学控制的,随着温度或硫代硫酸盐浓度的升高,金的氧化速度会加快. ...
... 石硫合剂浸金方法(LSSS)起源于国内,属于硫化物碱性氧化浸金技术范畴.国内学者选用多种类型金矿石进行了石硫合剂浸出试验研究,发现该方法具有无毒环保、浸金速度快、适应性强、金浸出率高以及对设备材料要求低等优点.傅平丰等[53]讨论了石硫合剂法浸金的基本原理,认为LSSS 法浸金反应需在通空气及氨存在的条件下进行,浸金体系中还需加入CuSO4及Na2SO3等活化剂和稳定剂,以提高Sx2-和S2O32-的稳定性,并强化浸金过程.LSSS体系中的有效浸金成分为CaSx和 CaS2O3,溶金过程符合多硫化物及硫代硫酸盐的浸金反应.郁能文等[54]对石硫合剂(LSSS)体系进行了电化学研究,认为添加氧化剂对体系电位影响剧烈,会造成体系的稳定性降低;试验测得了稳态极化曲线,求出了LSSS体系中金电极反应活化能为16.835 kJ/mol.靳冉公等[55]对含锑难冶炼金矿碱性湿法脱锑过程中金的浸出动力学进行了研究.结果表明:温度为20~70 ℃、硫化钠浓度为20~80 g/L范围内碱性硫化钠浸出锑金矿,金的表观活化能Ea=10.948 kJ/mol.郁能文等[54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
石硫合剂法浸金的原理、稳定性及应用研究进展
1
2012
... 石硫合剂浸金方法(LSSS)起源于国内,属于硫化物碱性氧化浸金技术范畴.国内学者选用多种类型金矿石进行了石硫合剂浸出试验研究,发现该方法具有无毒环保、浸金速度快、适应性强、金浸出率高以及对设备材料要求低等优点.傅平丰等[53]讨论了石硫合剂法浸金的基本原理,认为LSSS 法浸金反应需在通空气及氨存在的条件下进行,浸金体系中还需加入CuSO4及Na2SO3等活化剂和稳定剂,以提高Sx2-和S2O32-的稳定性,并强化浸金过程.LSSS体系中的有效浸金成分为CaSx和 CaS2O3,溶金过程符合多硫化物及硫代硫酸盐的浸金反应.郁能文等[54]对石硫合剂(LSSS)体系进行了电化学研究,认为添加氧化剂对体系电位影响剧烈,会造成体系的稳定性降低;试验测得了稳态极化曲线,求出了LSSS体系中金电极反应活化能为16.835 kJ/mol.靳冉公等[55]对含锑难冶炼金矿碱性湿法脱锑过程中金的浸出动力学进行了研究.结果表明:温度为20~70 ℃、硫化钠浓度为20~80 g/L范围内碱性硫化钠浸出锑金矿,金的表观活化能Ea=10.948 kJ/mol.郁能文等[54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
石硫合剂法浸金的原理、稳定性及应用研究进展
1
2012
... 石硫合剂浸金方法(LSSS)起源于国内,属于硫化物碱性氧化浸金技术范畴.国内学者选用多种类型金矿石进行了石硫合剂浸出试验研究,发现该方法具有无毒环保、浸金速度快、适应性强、金浸出率高以及对设备材料要求低等优点.傅平丰等[53]讨论了石硫合剂法浸金的基本原理,认为LSSS 法浸金反应需在通空气及氨存在的条件下进行,浸金体系中还需加入CuSO4及Na2SO3等活化剂和稳定剂,以提高Sx2-和S2O32-的稳定性,并强化浸金过程.LSSS体系中的有效浸金成分为CaSx和 CaS2O3,溶金过程符合多硫化物及硫代硫酸盐的浸金反应.郁能文等[54]对石硫合剂(LSSS)体系进行了电化学研究,认为添加氧化剂对体系电位影响剧烈,会造成体系的稳定性降低;试验测得了稳态极化曲线,求出了LSSS体系中金电极反应活化能为16.835 kJ/mol.靳冉公等[55]对含锑难冶炼金矿碱性湿法脱锑过程中金的浸出动力学进行了研究.结果表明:温度为20~70 ℃、硫化钠浓度为20~80 g/L范围内碱性硫化钠浸出锑金矿,金的表观活化能Ea=10.948 kJ/mol.郁能文等[54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
石硫合剂(LSSS)法浸金的电化学研究
2
1998
... 石硫合剂浸金方法(LSSS)起源于国内,属于硫化物碱性氧化浸金技术范畴.国内学者选用多种类型金矿石进行了石硫合剂浸出试验研究,发现该方法具有无毒环保、浸金速度快、适应性强、金浸出率高以及对设备材料要求低等优点.傅平丰等[53]讨论了石硫合剂法浸金的基本原理,认为LSSS 法浸金反应需在通空气及氨存在的条件下进行,浸金体系中还需加入CuSO4及Na2SO3等活化剂和稳定剂,以提高Sx2-和S2O32-的稳定性,并强化浸金过程.LSSS体系中的有效浸金成分为CaSx和 CaS2O3,溶金过程符合多硫化物及硫代硫酸盐的浸金反应.郁能文等[54]对石硫合剂(LSSS)体系进行了电化学研究,认为添加氧化剂对体系电位影响剧烈,会造成体系的稳定性降低;试验测得了稳态极化曲线,求出了LSSS体系中金电极反应活化能为16.835 kJ/mol.靳冉公等[55]对含锑难冶炼金矿碱性湿法脱锑过程中金的浸出动力学进行了研究.结果表明:温度为20~70 ℃、硫化钠浓度为20~80 g/L范围内碱性硫化钠浸出锑金矿,金的表观活化能Ea=10.948 kJ/mol.郁能文等[54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
... [54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
石硫合剂(LSSS)法浸金的电化学研究
2
1998
... 石硫合剂浸金方法(LSSS)起源于国内,属于硫化物碱性氧化浸金技术范畴.国内学者选用多种类型金矿石进行了石硫合剂浸出试验研究,发现该方法具有无毒环保、浸金速度快、适应性强、金浸出率高以及对设备材料要求低等优点.傅平丰等[53]讨论了石硫合剂法浸金的基本原理,认为LSSS 法浸金反应需在通空气及氨存在的条件下进行,浸金体系中还需加入CuSO4及Na2SO3等活化剂和稳定剂,以提高Sx2-和S2O32-的稳定性,并强化浸金过程.LSSS体系中的有效浸金成分为CaSx和 CaS2O3,溶金过程符合多硫化物及硫代硫酸盐的浸金反应.郁能文等[54]对石硫合剂(LSSS)体系进行了电化学研究,认为添加氧化剂对体系电位影响剧烈,会造成体系的稳定性降低;试验测得了稳态极化曲线,求出了LSSS体系中金电极反应活化能为16.835 kJ/mol.靳冉公等[55]对含锑难冶炼金矿碱性湿法脱锑过程中金的浸出动力学进行了研究.结果表明:温度为20~70 ℃、硫化钠浓度为20~80 g/L范围内碱性硫化钠浸出锑金矿,金的表观活化能Ea=10.948 kJ/mol.郁能文等[54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
... [54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
碱性硫化物浸出含锑金精矿中金的动力学研究
2
2019
... 石硫合剂浸金方法(LSSS)起源于国内,属于硫化物碱性氧化浸金技术范畴.国内学者选用多种类型金矿石进行了石硫合剂浸出试验研究,发现该方法具有无毒环保、浸金速度快、适应性强、金浸出率高以及对设备材料要求低等优点.傅平丰等[53]讨论了石硫合剂法浸金的基本原理,认为LSSS 法浸金反应需在通空气及氨存在的条件下进行,浸金体系中还需加入CuSO4及Na2SO3等活化剂和稳定剂,以提高Sx2-和S2O32-的稳定性,并强化浸金过程.LSSS体系中的有效浸金成分为CaSx和 CaS2O3,溶金过程符合多硫化物及硫代硫酸盐的浸金反应.郁能文等[54]对石硫合剂(LSSS)体系进行了电化学研究,认为添加氧化剂对体系电位影响剧烈,会造成体系的稳定性降低;试验测得了稳态极化曲线,求出了LSSS体系中金电极反应活化能为16.835 kJ/mol.靳冉公等[55]对含锑难冶炼金矿碱性湿法脱锑过程中金的浸出动力学进行了研究.结果表明:温度为20~70 ℃、硫化钠浓度为20~80 g/L范围内碱性硫化钠浸出锑金矿,金的表观活化能Ea=10.948 kJ/mol.郁能文等[54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
... [55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
碱性硫化物浸出含锑金精矿中金的动力学研究
2
2019
... 石硫合剂浸金方法(LSSS)起源于国内,属于硫化物碱性氧化浸金技术范畴.国内学者选用多种类型金矿石进行了石硫合剂浸出试验研究,发现该方法具有无毒环保、浸金速度快、适应性强、金浸出率高以及对设备材料要求低等优点.傅平丰等[53]讨论了石硫合剂法浸金的基本原理,认为LSSS 法浸金反应需在通空气及氨存在的条件下进行,浸金体系中还需加入CuSO4及Na2SO3等活化剂和稳定剂,以提高Sx2-和S2O32-的稳定性,并强化浸金过程.LSSS体系中的有效浸金成分为CaSx和 CaS2O3,溶金过程符合多硫化物及硫代硫酸盐的浸金反应.郁能文等[54]对石硫合剂(LSSS)体系进行了电化学研究,认为添加氧化剂对体系电位影响剧烈,会造成体系的稳定性降低;试验测得了稳态极化曲线,求出了LSSS体系中金电极反应活化能为16.835 kJ/mol.靳冉公等[55]对含锑难冶炼金矿碱性湿法脱锑过程中金的浸出动力学进行了研究.结果表明:温度为20~70 ℃、硫化钠浓度为20~80 g/L范围内碱性硫化钠浸出锑金矿,金的表观活化能Ea=10.948 kJ/mol.郁能文等[54]和靳冉公等[55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
... [55]研究表明,在考察范围内,金浸出主要受反应物扩散过程控制.这与Anderson[51]和Sitando等[52]的研究结果(金溶解属于化学控制过程)不同,推测原因可能是浸出体系中溶金硫化物离子、氧化催化剂及杂质离子等成分不同造成的,需要进一步研究确定. ...
硫代硫酸盐浸金各因素影响研究现状
1
2018
... 大量研究报道了硫化物对金在氰化过程中溶解和钝化层形成的电化学行为的影响[56-59].在碱性溶液中金属硫化物会氧化溶解,产生一些含硫阴离子,使金表面钝化,从而延缓浸出过程,造成金的浸出率降低. ...
硫代硫酸盐浸金各因素影响研究现状
1
2018
... 大量研究报道了硫化物对金在氰化过程中溶解和钝化层形成的电化学行为的影响[56-59].在碱性溶液中金属硫化物会氧化溶解,产生一些含硫阴离子,使金表面钝化,从而延缓浸出过程,造成金的浸出率降低. ...
Effect of common associated sulfide minerals on thiosulfate leaching of gold and the role of humic acid additive
0
2017
A review on electro-chemical dissolution and passivation of gold during cyanidation in presence of sulphides and oxides
0
2017
硫代硫酸钠电化学氧化过程中 Au(111)晶面形貌研究及其机理分析
1
2019
... 大量研究报道了硫化物对金在氰化过程中溶解和钝化层形成的电化学行为的影响[56-59].在碱性溶液中金属硫化物会氧化溶解,产生一些含硫阴离子,使金表面钝化,从而延缓浸出过程,造成金的浸出率降低. ...
硫代硫酸钠电化学氧化过程中 Au(111)晶面形貌研究及其机理分析
1
2019
... 大量研究报道了硫化物对金在氰化过程中溶解和钝化层形成的电化学行为的影响[56-59].在碱性溶液中金属硫化物会氧化溶解,产生一些含硫阴离子,使金表面钝化,从而延缓浸出过程,造成金的浸出率降低. ...
A SERS spectroelectrochemical investigation of the interaction of sulfide species with gold surfaces
1
2008
... Parker等[60]观察到硫化物在金表面上的还原发生在电位为-0.68 V和-0.94 V的2个峰值处,认为在较高电位处的峰值代表了零价硫转化为多硫化物离子和多硫化物离子转化为硫化物离子.Zhou等[61]研究发现,在碱性硫脲溶液中,当电位大于0.42 V时,金电极的表面就会出现钝化,而添加Na2SiO3可以促进金的电化学溶解.Breuer等[62] 和 Jeffrey[63]研究得出,含铜和氨的硫代硫酸盐溶液中金的浸出动力学遵循化学控制模型,金表面钝化是导致浸出率降低的主要原因.Senanayake[64]研究发现,金的整体溶解与收缩核模型一致,证实了金表面会形成吸附层.Wierse等[65]利用电化学技术揭示了硫吸附层在金电极上的形成机理,研究认为,在多硫化物溶液中硫化物离子通过硫键的裂解和单个硫原子的吸附而形成了硫吸附层. ...
Electrochemical behavior of gold and its associated minerals in alkaline thiourea solutions
1
2018
... Parker等[60]观察到硫化物在金表面上的还原发生在电位为-0.68 V和-0.94 V的2个峰值处,认为在较高电位处的峰值代表了零价硫转化为多硫化物离子和多硫化物离子转化为硫化物离子.Zhou等[61]研究发现,在碱性硫脲溶液中,当电位大于0.42 V时,金电极的表面就会出现钝化,而添加Na2SiO3可以促进金的电化学溶解.Breuer等[62] 和 Jeffrey[63]研究得出,含铜和氨的硫代硫酸盐溶液中金的浸出动力学遵循化学控制模型,金表面钝化是导致浸出率降低的主要原因.Senanayake[64]研究发现,金的整体溶解与收缩核模型一致,证实了金表面会形成吸附层.Wierse等[65]利用电化学技术揭示了硫吸附层在金电极上的形成机理,研究认为,在多硫化物溶液中硫化物离子通过硫键的裂解和单个硫原子的吸附而形成了硫吸附层. ...
Thiosulfate leaching kinetics of gold in the presence of copper and ammonia
1
2000
... Parker等[60]观察到硫化物在金表面上的还原发生在电位为-0.68 V和-0.94 V的2个峰值处,认为在较高电位处的峰值代表了零价硫转化为多硫化物离子和多硫化物离子转化为硫化物离子.Zhou等[61]研究发现,在碱性硫脲溶液中,当电位大于0.42 V时,金电极的表面就会出现钝化,而添加Na2SiO3可以促进金的电化学溶解.Breuer等[62] 和 Jeffrey[63]研究得出,含铜和氨的硫代硫酸盐溶液中金的浸出动力学遵循化学控制模型,金表面钝化是导致浸出率降低的主要原因.Senanayake[64]研究发现,金的整体溶解与收缩核模型一致,证实了金表面会形成吸附层.Wierse等[65]利用电化学技术揭示了硫吸附层在金电极上的形成机理,研究认为,在多硫化物溶液中硫化物离子通过硫键的裂解和单个硫原子的吸附而形成了硫吸附层. ...
Kinetic aspects of gold and silver leaching in ammonia-thiosulfate solutions
1
2001
... Parker等[60]观察到硫化物在金表面上的还原发生在电位为-0.68 V和-0.94 V的2个峰值处,认为在较高电位处的峰值代表了零价硫转化为多硫化物离子和多硫化物离子转化为硫化物离子.Zhou等[61]研究发现,在碱性硫脲溶液中,当电位大于0.42 V时,金电极的表面就会出现钝化,而添加Na2SiO3可以促进金的电化学溶解.Breuer等[62] 和 Jeffrey[63]研究得出,含铜和氨的硫代硫酸盐溶液中金的浸出动力学遵循化学控制模型,金表面钝化是导致浸出率降低的主要原因.Senanayake[64]研究发现,金的整体溶解与收缩核模型一致,证实了金表面会形成吸附层.Wierse等[65]利用电化学技术揭示了硫吸附层在金电极上的形成机理,研究认为,在多硫化物溶液中硫化物离子通过硫键的裂解和单个硫原子的吸附而形成了硫吸附层. ...
Analysis of reaction kinetics,speciation and mechanism of gold leaching and thiosulfate oxidation by ammoniacal copper(Ⅱ)solutions
1
2004
... Parker等[60]观察到硫化物在金表面上的还原发生在电位为-0.68 V和-0.94 V的2个峰值处,认为在较高电位处的峰值代表了零价硫转化为多硫化物离子和多硫化物离子转化为硫化物离子.Zhou等[61]研究发现,在碱性硫脲溶液中,当电位大于0.42 V时,金电极的表面就会出现钝化,而添加Na2SiO3可以促进金的电化学溶解.Breuer等[62] 和 Jeffrey[63]研究得出,含铜和氨的硫代硫酸盐溶液中金的浸出动力学遵循化学控制模型,金表面钝化是导致浸出率降低的主要原因.Senanayake[64]研究发现,金的整体溶解与收缩核模型一致,证实了金表面会形成吸附层.Wierse等[65]利用电化学技术揭示了硫吸附层在金电极上的形成机理,研究认为,在多硫化物溶液中硫化物离子通过硫键的裂解和单个硫原子的吸附而形成了硫吸附层. ...
Elec-trochemical properties of sulfur adsorbed on gold electrodes
1
1978
... Parker等[60]观察到硫化物在金表面上的还原发生在电位为-0.68 V和-0.94 V的2个峰值处,认为在较高电位处的峰值代表了零价硫转化为多硫化物离子和多硫化物离子转化为硫化物离子.Zhou等[61]研究发现,在碱性硫脲溶液中,当电位大于0.42 V时,金电极的表面就会出现钝化,而添加Na2SiO3可以促进金的电化学溶解.Breuer等[62] 和 Jeffrey[63]研究得出,含铜和氨的硫代硫酸盐溶液中金的浸出动力学遵循化学控制模型,金表面钝化是导致浸出率降低的主要原因.Senanayake[64]研究发现,金的整体溶解与收缩核模型一致,证实了金表面会形成吸附层.Wierse等[65]利用电化学技术揭示了硫吸附层在金电极上的形成机理,研究认为,在多硫化物溶液中硫化物离子通过硫键的裂解和单个硫原子的吸附而形成了硫吸附层. ...
Gold passivation by sulfur species:A molecular picture
1
2019
... Zia等[66]研究了硫化物和硫代硫酸盐对金的钝化作用,用密度泛函理论(Density Function Theory,DFT)方法计算了不同含硫离子与金表面的相互作用能.结果表明,钝化膜的形成主要是硫化物、多硫化物、四硫酸盐和亚硫酸盐与金表面相互作用的结果,硫化物与金表面的相互作用能大于金与其他硫化物之间的相互作用能,说明硫化物离子比硫代硫酸盐更容易被吸附.Zelinsky等[67]应用EQCM对氨态硫代硫酸盐溶液中金的浸出进行了研究,结果表明,硫代硫酸盐分解产生富硫层使金电极钝化,降低了金的浸出率,而硫代硫酸盐的降解产物主要是四亚硫酸盐、硫酸盐和单质硫等. ...
EQCM study of the dissolution of gold in thiosulfate solutions
1
2013
... Zia等[66]研究了硫化物和硫代硫酸盐对金的钝化作用,用密度泛函理论(Density Function Theory,DFT)方法计算了不同含硫离子与金表面的相互作用能.结果表明,钝化膜的形成主要是硫化物、多硫化物、四硫酸盐和亚硫酸盐与金表面相互作用的结果,硫化物与金表面的相互作用能大于金与其他硫化物之间的相互作用能,说明硫化物离子比硫代硫酸盐更容易被吸附.Zelinsky等[67]应用EQCM对氨态硫代硫酸盐溶液中金的浸出进行了研究,结果表明,硫代硫酸盐分解产生富硫层使金电极钝化,降低了金的浸出率,而硫代硫酸盐的降解产物主要是四亚硫酸盐、硫酸盐和单质硫等. ...
Identification of surface species that inhibit and passivate thiosulfate leaching of gold
1
2008
... Jeffrey等[68]和Nicol等[69]等利用电化学和SERS(表面增强拉曼光谱,Surface Enhanced Raman Scattering)技术研究了阻碍金在硫代硫酸盐溶液中溶解的钝化物质的组成.结果表明,硫代硫酸盐的氧化使金表面形成硫、多硫化物,并使多硫酸盐吸附在金表面.Huergo等[70]开展了用硫化钠溶液还原金(Ⅲ)合成金纳米结构的研究,发现钝化层主要由单体硫、多硫化物和部分单质硫组成,钝化层产物中既没有Au2S,也没有其他金的配合物存在. ...
Surface enhanced Raman spectroscopy studies of the passive layer formation in gold leaching from thiosulfate solutions in the presence of cupric ion
1
2014
... Jeffrey等[68]和Nicol等[69]等利用电化学和SERS(表面增强拉曼光谱,Surface Enhanced Raman Scattering)技术研究了阻碍金在硫代硫酸盐溶液中溶解的钝化物质的组成.结果表明,硫代硫酸盐的氧化使金表面形成硫、多硫化物,并使多硫酸盐吸附在金表面.Huergo等[70]开展了用硫化钠溶液还原金(Ⅲ)合成金纳米结构的研究,发现钝化层主要由单体硫、多硫化物和部分单质硫组成,钝化层产物中既没有Au2S,也没有其他金的配合物存在. ...
New insight into the chemical nature of the plasmonic nanostructures synthesized by the reduction of Au(Ⅲ)with sulfide species
1
2017
... Jeffrey等[68]和Nicol等[69]等利用电化学和SERS(表面增强拉曼光谱,Surface Enhanced Raman Scattering)技术研究了阻碍金在硫代硫酸盐溶液中溶解的钝化物质的组成.结果表明,硫代硫酸盐的氧化使金表面形成硫、多硫化物,并使多硫酸盐吸附在金表面.Huergo等[70]开展了用硫化钠溶液还原金(Ⅲ)合成金纳米结构的研究,发现钝化层主要由单体硫、多硫化物和部分单质硫组成,钝化层产物中既没有Au2S,也没有其他金的配合物存在. ...
某难浸金矿的次氯酸盐法直接浸金试验研究
1
2014
... 关于含金硫化矿碱性氧化浸出工艺的试验研究较多,大部分都能取得较好的浸金效果.李超等[71]研究了NaClO-NaCl 浓度和反应时间等条件对浸金率的影响,并采用 X-射线衍射、XRF、SEM 和 EDS 能谱等测试方法对金精矿和浸出渣进行了表征,简要分析了浸出机理.试验结果表明:精矿中的金在pH<8、电位大于900 mV的条件下,能够被浸出并形成稳定配合物存在于溶液中,最佳试验条件为[NaCl]=50 g/L,[NaClO]=200 g/L,液固比=20∶1,反应3 h后,金浸出率可达96.26%,脱硫率达 98 %以上. ...
某难浸金矿的次氯酸盐法直接浸金试验研究
1
2014
... 关于含金硫化矿碱性氧化浸出工艺的试验研究较多,大部分都能取得较好的浸金效果.李超等[71]研究了NaClO-NaCl 浓度和反应时间等条件对浸金率的影响,并采用 X-射线衍射、XRF、SEM 和 EDS 能谱等测试方法对金精矿和浸出渣进行了表征,简要分析了浸出机理.试验结果表明:精矿中的金在pH<8、电位大于900 mV的条件下,能够被浸出并形成稳定配合物存在于溶液中,最佳试验条件为[NaCl]=50 g/L,[NaClO]=200 g/L,液固比=20∶1,反应3 h后,金浸出率可达96.26%,脱硫率达 98 %以上. ...
Study on the oxygen pressure alkaline leaching of gold with generated thiosulfate from sulfur oxidation
1
2018
... Melashvili等[48]对硫铁矿氧化过程中金的溶解情况进行了研究,结果表明,黄铁矿中硫首先被氧化成单质硫,再被氧化成硫代硫酸盐和其他硫氧阴离子,在pH<12的条件下,金的最高回收率达到96%.Xu等[72]以腐殖酸为添加剂,采用加压氧化法预处理硫化矿,利用硫氧化过程中生成的硫代硫酸盐进行浸金,金的回收率达到83.6%. ...
Electrochemical recovery of gold from concentrate by using sulfur-graphite electrode as the leaching agent source
1
2018
... Nadirov等[73]制备了一种特殊的“硫/石墨”电极并使用这种电极来产生含硫的浸金剂,在碱性溶液中提取金,金的回收率达到了93%.Yang等[33]采用硫和硫化钠在加压水热条件下反应生成多硫化钠溶液,并使用该多硫化钠溶液作为浸金剂进行含金矿石的浸出,取得了较好的浸出效果,该方法对试验金矿石样品的金浸出率达到85%.唐云等[74]采用碱性热压预处理—硫代硫酸盐浸出含碳质微细粒浸染型难选原生金矿,试验结果表明,在磨矿细度为-0.025 mm粒级占82%,预处理温度为160 ℃、预处理时间为2 h、助氧剂TW用量为300 g/t、氧压为1.6 MPa、pH=12的碱性热压氧化条件下以及硫代硫酸钠用量为0.12 mol/L、硫酸铵用量为0.075 mol/L、硫酸铜用量为0.02 mol/L、pH=9、浸出时间为4 h、矿浆液固比为3∶1的浸出条件下,金浸出率为88.76%. ...
微细浸染金矿碱性热压预处理—硫代硫酸钠浸金
1
2016
... Nadirov等[73]制备了一种特殊的“硫/石墨”电极并使用这种电极来产生含硫的浸金剂,在碱性溶液中提取金,金的回收率达到了93%.Yang等[33]采用硫和硫化钠在加压水热条件下反应生成多硫化钠溶液,并使用该多硫化钠溶液作为浸金剂进行含金矿石的浸出,取得了较好的浸出效果,该方法对试验金矿石样品的金浸出率达到85%.唐云等[74]采用碱性热压预处理—硫代硫酸盐浸出含碳质微细粒浸染型难选原生金矿,试验结果表明,在磨矿细度为-0.025 mm粒级占82%,预处理温度为160 ℃、预处理时间为2 h、助氧剂TW用量为300 g/t、氧压为1.6 MPa、pH=12的碱性热压氧化条件下以及硫代硫酸钠用量为0.12 mol/L、硫酸铵用量为0.075 mol/L、硫酸铜用量为0.02 mol/L、pH=9、浸出时间为4 h、矿浆液固比为3∶1的浸出条件下,金浸出率为88.76%. ...
微细浸染金矿碱性热压预处理—硫代硫酸钠浸金
1
2016
... Nadirov等[73]制备了一种特殊的“硫/石墨”电极并使用这种电极来产生含硫的浸金剂,在碱性溶液中提取金,金的回收率达到了93%.Yang等[33]采用硫和硫化钠在加压水热条件下反应生成多硫化钠溶液,并使用该多硫化钠溶液作为浸金剂进行含金矿石的浸出,取得了较好的浸出效果,该方法对试验金矿石样品的金浸出率达到85%.唐云等[74]采用碱性热压预处理—硫代硫酸盐浸出含碳质微细粒浸染型难选原生金矿,试验结果表明,在磨矿细度为-0.025 mm粒级占82%,预处理温度为160 ℃、预处理时间为2 h、助氧剂TW用量为300 g/t、氧压为1.6 MPa、pH=12的碱性热压氧化条件下以及硫代硫酸钠用量为0.12 mol/L、硫酸铵用量为0.075 mol/L、硫酸铜用量为0.02 mol/L、pH=9、浸出时间为4 h、矿浆液固比为3∶1的浸出条件下,金浸出率为88.76%. ...
改性石硫合剂提取贵金属的方法
1
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
改性石硫合剂提取贵金属的方法
1
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
一种新的溶金银试剂—石硫合剂
1
1994
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
一种新的溶金银试剂—石硫合剂
1
1994
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
石硫合剂(LSSS)浸金的研究
1
2005
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
石硫合剂(LSSS)浸金的研究
1
2005
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
石硫合剂浸金体系的探讨
1
2009
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
石硫合剂浸金体系的探讨
1
2009
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
含硫试剂对某难处理精金矿的浸出研究
1
2008
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
含硫试剂对某难处理精金矿的浸出研究
1
2008
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
改性石硫合剂(ML)浸金试剂稳定性研究
1
2008
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
改性石硫合剂(ML)浸金试剂稳定性研究
1
2008
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
某金矿石的石硫加碱催化合剂法浸金研究
1
2013
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
某金矿石的石硫加碱催化合剂法浸金研究
1
2013
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
载金硫化物焙烧—自浸出过程研究
1
2015
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
载金硫化物焙烧—自浸出过程研究
1
2015
... 兰新哲等[75]和张箭等[76]研究发现石硫合剂实质上就是多硫化物和硫代硫酸盐的混合体,使用石硫合剂,金浸出率可以达到96%以上,浸出周期为常规氰化法的1/8~1/2.陈江安等[77-78]提出在石硫合剂浸金过程中,添加一定量的NaCl可提高浸出率并降低生产成本.周军等[79-80]对改性石硫合剂的稳定性进行了研究,并采用石硫合剂浸金工艺对陕西镇安金矿含碳砷细微金矿石进行浸出处理,原生矿浸出率达到 90%以上,尾矿金品位降到0.4 g/t以下.刘有才等[81]对矿石进行了石硫加碱催化合剂的搅拌浸金研究,确定最优试验条件为:液固比为2.0,所用氧化剂为H2O2,浓度为0.02 mol/L,pH值为12~13,搅拌时间为3.5~4.0 h.此条件下金浸出率可达72.6%.赵留成等[82]采用焙烧—自浸出工艺提取载金硫化物中的金,在氮气气氛下焙烧载金硫化物,使其中的主要载金硫化矿物黄铁矿和其他硫化矿物反应生成单质硫,再添加适量的石灰与单质硫合成石硫合剂,浸出焙砂中金.在氮气流量为1 L/min、焙烧温度为800 ℃和焙烧时间为60 min的条件下,试样中单质硫的转化率达到42.53%,金浸出率达到88.70%. ...
某金矿石的改性石硫合剂法浸金研究
1
2016
... 冯杰等[83]采用改性石硫合剂法进行某金矿石的浸金研究,当矿浆液固比为2∶1、磨矿细度为-45 μm占55%、矿浆pH值为11.0、浸出时间为6 h、改性石硫合剂用量为8 kg/t及H2O2投加量为3.33 kg/t时,金的浸出率为89.81%,比氰化浸出提高了16.35%. ...
某金矿石的改性石硫合剂法浸金研究
1
2016
... 冯杰等[83]采用改性石硫合剂法进行某金矿石的浸金研究,当矿浆液固比为2∶1、磨矿细度为-45 μm占55%、矿浆pH值为11.0、浸出时间为6 h、改性石硫合剂用量为8 kg/t及H2O2投加量为3.33 kg/t时,金的浸出率为89.81%,比氰化浸出提高了16.35%. ...
Gold bearing arsenopyrite and pyrite in refractory ores:Analytical refinements and new understanding of gold mineralogy
1
2007
... 众所周知,绝大部分金矿均以硫化矿物为载金矿物,金通常与黄铁矿、毒砂、磁黄铁矿、黄铜矿和脉石等载体矿物伴生或包裹在其中,而且大部分属于微细粒浸染型难处理金矿[84-87].从地质角度来看,金与硫化矿物共生关系密切;从化学角度来看,Au元素和S元素具有相亲性,即在一定条件下,金和硫会发生化学反应.而金的嵌布状态(包括粒度、结构、构造和共生关系等特征)应该与金、硫化矿及脉石矿物在地质作用过程中发生的物理化学过程有关.了解了含金硫化矿在自然界中的形成过程,将对该类型金矿的提取回收具有一定的启发作用. ...
Process mineralogy characteristics of acid leaching residue produced in low-temperature roasting acid leaching pretreatment process of refractory gold concentrates
0
2018
混合非氰药剂对微细浸染型金矿浸出的影响研究
0
2015
混合非氰药剂对微细浸染型金矿浸出的影响研究
0
2015
卡林型金矿微生物预氧化处理技术研究现状
1
2012
... 众所周知,绝大部分金矿均以硫化矿物为载金矿物,金通常与黄铁矿、毒砂、磁黄铁矿、黄铜矿和脉石等载体矿物伴生或包裹在其中,而且大部分属于微细粒浸染型难处理金矿[84-87].从地质角度来看,金与硫化矿物共生关系密切;从化学角度来看,Au元素和S元素具有相亲性,即在一定条件下,金和硫会发生化学反应.而金的嵌布状态(包括粒度、结构、构造和共生关系等特征)应该与金、硫化矿及脉石矿物在地质作用过程中发生的物理化学过程有关.了解了含金硫化矿在自然界中的形成过程,将对该类型金矿的提取回收具有一定的启发作用. ...
卡林型金矿微生物预氧化处理技术研究现状
1
2012
... 众所周知,绝大部分金矿均以硫化矿物为载金矿物,金通常与黄铁矿、毒砂、磁黄铁矿、黄铜矿和脉石等载体矿物伴生或包裹在其中,而且大部分属于微细粒浸染型难处理金矿[84-87].从地质角度来看,金与硫化矿物共生关系密切;从化学角度来看,Au元素和S元素具有相亲性,即在一定条件下,金和硫会发生化学反应.而金的嵌布状态(包括粒度、结构、构造和共生关系等特征)应该与金、硫化矿及脉石矿物在地质作用过程中发生的物理化学过程有关.了解了含金硫化矿在自然界中的形成过程,将对该类型金矿的提取回收具有一定的启发作用. ...
Thermal decomposition behavior of pyrite in a microwave field and feasibility of gold leaching with generated elemental sulfur from the decomposition of gold-bearing sulfides
1
2018
... 一些学者研究了高温下金和硫的结合情况,结果表明在高温下金与硫能结合并以稳定形式存在.Anderson等[42]研究了温度对碱性硫化物体系中AuS-络合物稳定性的影响,Eh-pH图表明,高温下硫化金的稳定区域相对较大,因此,提高回火温度有利于金在碱性硫化物溶液中的浸出.Zhang等[88]研究提出,微波热解过程中含金硫化物生成的单质硫可以用于从自身提取金.微波预处理在无氧条件下不仅产生了用于合成浸出剂的单质硫,而且释放了包裹在硫化矿物中的金.这些研究虽然温度尚不能达到地壳运动过程中的高温,但至少说明高温对金、硫赋存状态的影响很大.Sun等[89] 通过对中国东北白云金矿的黄铁矿进行S同位素原位分析研究得出,黄铁矿及裂隙中的可见金是从富含金属的岩浆中析出的,而不是变质黄铁矿二次搬运来的.这说明硫化矿很可能在岩浆热液作用的特定条件下与金形成过金硫化合物. ...
Trace element contents and in situ sulfur isotope analyses of pyrite in the Baiyun gold deposit,NE China:Implication for the genesis of intrusion-related gold deposits
1
2020
... 一些学者研究了高温下金和硫的结合情况,结果表明在高温下金与硫能结合并以稳定形式存在.Anderson等[42]研究了温度对碱性硫化物体系中AuS-络合物稳定性的影响,Eh-pH图表明,高温下硫化金的稳定区域相对较大,因此,提高回火温度有利于金在碱性硫化物溶液中的浸出.Zhang等[88]研究提出,微波热解过程中含金硫化物生成的单质硫可以用于从自身提取金.微波预处理在无氧条件下不仅产生了用于合成浸出剂的单质硫,而且释放了包裹在硫化矿物中的金.这些研究虽然温度尚不能达到地壳运动过程中的高温,但至少说明高温对金、硫赋存状态的影响很大.Sun等[89] 通过对中国东北白云金矿的黄铁矿进行S同位素原位分析研究得出,黄铁矿及裂隙中的可见金是从富含金属的岩浆中析出的,而不是变质黄铁矿二次搬运来的.这说明硫化矿很可能在岩浆热液作用的特定条件下与金形成过金硫化合物. ...
硫代硫酸盐浸金溶液中金的分析及回收
1
2011
... (5)金溶出后含金贵液的提金工艺及无害化处理.根据文献资料[90-92]和曾开展的相关试验,由于金与多硫化物或硫代硫酸盐形成的金硫配合物体积大、电荷高,因此,常规的活性碳吸附工艺并不能取得很好的金吸附效果,必须采用其他合适方法或者改善活性碳吸附性能,应加强这方面的研究工作. ...
硫代硫酸盐浸金溶液中金的分析及回收
1
2011
... (5)金溶出后含金贵液的提金工艺及无害化处理.根据文献资料[90-92]和曾开展的相关试验,由于金与多硫化物或硫代硫酸盐形成的金硫配合物体积大、电荷高,因此,常规的活性碳吸附工艺并不能取得很好的金吸附效果,必须采用其他合适方法或者改善活性碳吸附性能,应加强这方面的研究工作. ...
活性炭吸附回收浸出液中金络合物的研究进展
0
2019
活性炭吸附回收浸出液中金络合物的研究进展
0
2019
Towards a more environmentally friendly process for gold:Models on gold adsorption onto activated carbon from ammoniacal thiosulfate solutions
1
2007
... (5)金溶出后含金贵液的提金工艺及无害化处理.根据文献资料[90-92]和曾开展的相关试验,由于金与多硫化物或硫代硫酸盐形成的金硫配合物体积大、电荷高,因此,常规的活性碳吸附工艺并不能取得很好的金吸附效果,必须采用其他合适方法或者改善活性碳吸附性能,应加强这方面的研究工作. ...






 甘公网安备 62010202000672号
甘公网安备 62010202000672号